헛소리 시험공부가 너무 즐거워! 하하!
- 도체vs반도체vs절연체 [2-1~2-2]
- 도체 :
전도도 10^6 이상, 반도체 10^-3~10^2, 절연체 10^-10 이하
도체의 전도도 공식 = nqu (carrier 농도 * 전하량 * 이동도),
온도에 반비례 (why? 이동도 감소, Thermal agitation(진동) 때문에 전자가 산란)
-> 이 현상 이용 : 열전대(Thermocouples) – 전자가 hot -> cold 이동, 차가운 곳에 전자 = (-)극 형성,
두 개의 다른 금속을 연결하여 온도차에 비례하는 전압을 측정 -> seeback effect
- 절연체(부도체) :
전도도 10^-10~10^-16, 유전체 층으로 활용 Capacitor, 전기장 걸리면 분극.
분극이란 원자 내부에서 양전하와 음전하가 분리되어 전극 표면의 전하를 생성함.
전하량은 재료의 유전상수 값에 의해 결정됨. C=Q/V, C=단위부피당 전하 저장 능력
- 반도체
전도도 10^-4 ~ 10^4 범위, 전도도 -> nqu에서 nq(u_n+u_p), mobillity는 전자가 높음.
온도가 올라갈수록 캐리어 양 증가 -> 전도도 증가 (금속과 반대특성)
내인성 반도체 (Intrinsic) : 14족 원소로만 이루어짐. Si, Ge, GaAs
외인성 반도체 (extrinsic) : 불순물 원자(dopants)를 넣어서 캐리어 농도를 높임. 전도도 좋아짐.
-> p형 : 3족 원소(B, Al, Ga)를 doping, 홀이 다수캐리어
-> n형 : 5족 원소(P, As, Sb)를 doping, 전자가 다수캐리어
- 분자 구조 그리기 (C2H6, C4H6, C2H2), elctron-dot, line-bond [3-1] -> *2차원의 한계
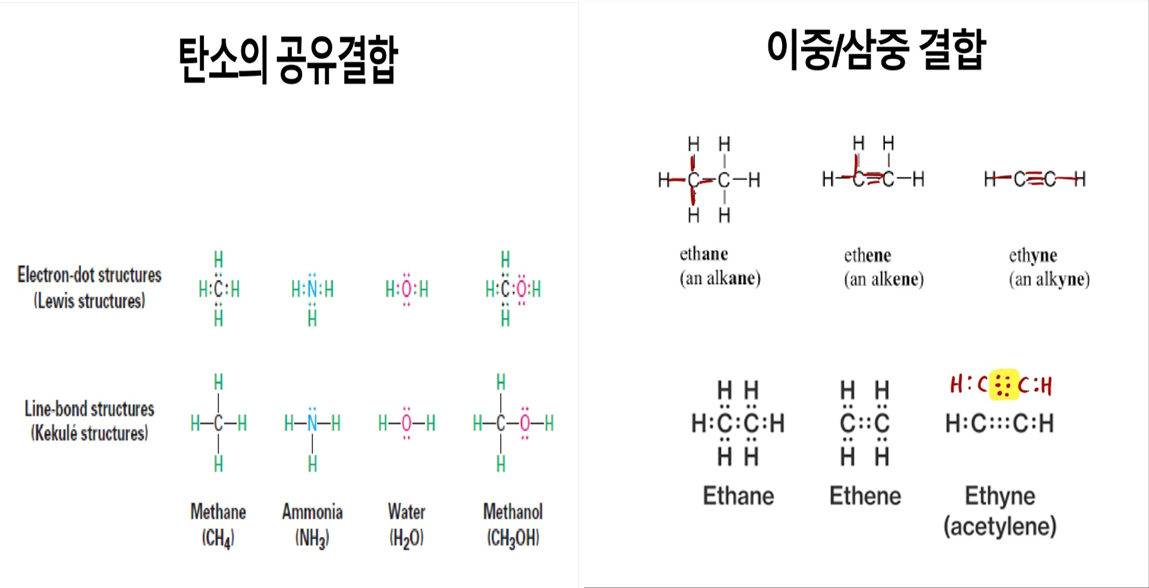
3. 원자, 분자의 결합 방식 [3-1]
- 오비탈
전자의 존재 확률을 나타냄. 1차결합은 오비탈 전자가 이동 (ex이온결합) 또는 공유(공유결합) 2차결합은 양전하와 음전하 사이의 미묘한 인력 (pi결합), 물리적결합x, 화학적결합o
- 공유결합
1차 결합으로 에너지 가장 안정, orbital의 overlap, 가장 에너지가 낮은 결합 길이와 각도 형성. 결합에 참여하지 않는 전자들은 “비공유전자쌍”의 형태로 존재함.
탄소는 원래 1s2 2s2 2p2로 전자가 배치되어야 하는데, 4개의 최외곽전자를 맞추기 위해 1s2 2s1 2p3, 또는 sp3 하이브리드화로 설명.
- 이중/삼중결합 (*시그마 결합과 파이 결합)
- 시그마 결합 :
2, 3중 결합 중 최소 1개 있어야 하고, 정면 중첩, 직접적인 오비탈의 겹침에 의한 결합,
일반적 공유 결합. 비교적 강력함.
- 파이 결합 :
2, 3중결합에서 시그마 결합 제외한 나머지 결합, 측면 중첩에 의한 결합, 특수한 결합
-> 결합력은 약하지만 전자가 움직일 수 있음(더 자유로워짐), 전기전도도 생김. 유기 “반도체”
토막지식
- 유기물 : 탄소 원자가 H, O, N, S, 할로젠 원소와 결합하여 만들어진 화합물
- 페르미레벨 : 특정 에너지 레벨에 전자가 존재할 확률
- 공유결합의 극성 : 전기음성도에 의해 결정, 우측 상방으로 갈수록 전기음성도가 커지는 경향성 (F, Cl, O) 숫자가 클 수록(차이가 많이 날수록) 전자를 더 잘 끌어당김.
- 에탄(C2H6), 대칭구조, 회전가능 (Symmetric rotate)
4. 작용기 : 공통의 화학적 특성을 지니는 유기화합물의 공통된 원자단 또는 결합양식. 모든 유기물은 작용기에 의해 결정 - 형광펜 칠해놓은것은 암기해아함
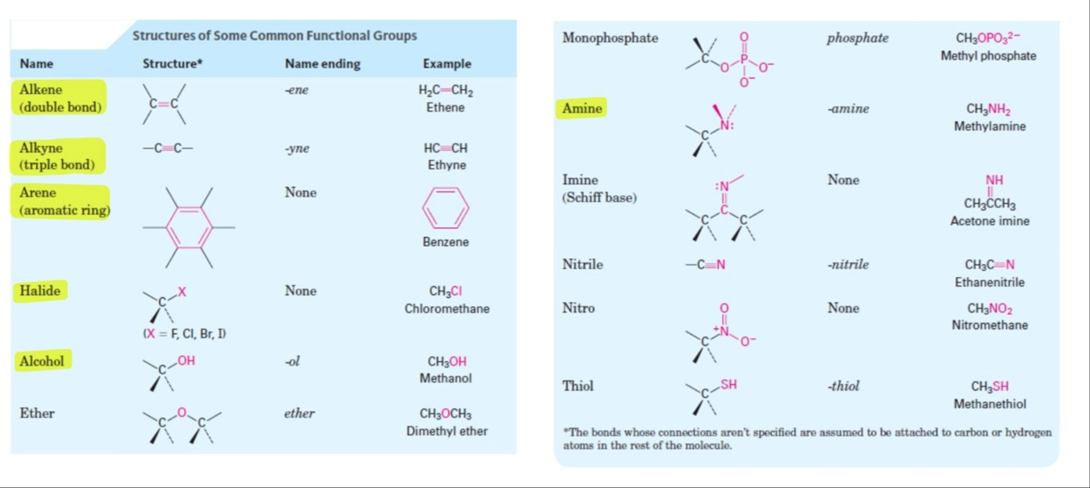
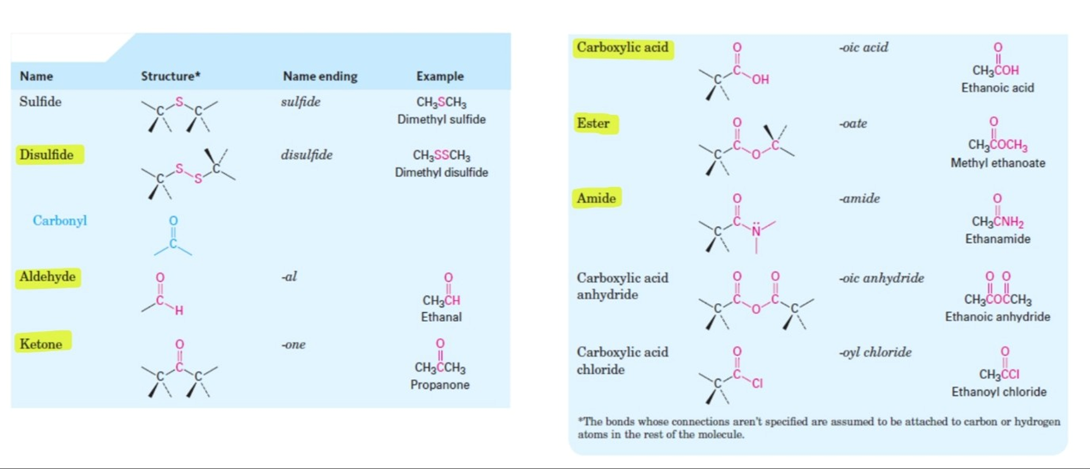
5. 산, 염기의 정의 (브뢴스테드-로우리, 루이스)
- 브뢴스테드 로우리 산 : 수소 이온(H+)을 제공하는 물질
브뢴스테드 로우리 염기 : 수소 이온(H+)을 받는 물질
ex) HCl + H20 -> H3O+ + Cl- 에서 HCL은 산, H20는 염기
* 심화
- 유전 손실 :
1. Aging effect : 시간이 지남에 따라 유전 특성이 저하되고 절연 내력이 감소함
2 .Intrinsic breakdown : 유전체에 있는 자유전자가 전기장의 영향으로 VB -> CB로 올라가서 이온화됨.
3. Thermal breakdown : 고주파에서 유전 손실이 커지면서 온도 증가 -> 전도도 증가, 가열된 Hotspot에서 국부적 breakdown이 일어나고, 반대 전극에 연결되는 conducting channel 형성
4. Internal discharge : 공극, 균열 또는 기공에서 발생하는 부분 방전 현상. Field가 충분히 크면 다공성 세라믹에 부분 방전 발생, 공극의 내부 표면을 부식시키고 절연체를 국부적으로 녹일 수 있음.
지금까지 29개 주제중에 5개 정리하고 24개 남았따.. 시험은 목요일..
- Polymers 특성 (인장 강도 등)
- 열 가소성 vs 열 경화성
- 고분자의 구조(backbone, side-chain, 작용기)
- 고분자의 분자량 계산 (중합도, 분자량, 수 평균, 중량 평균)
- 고분자 architectrue (Random, Alternating, Block)
- 고분자 블렌드 vs 블록공중합체 비교
- Conjugated 뜻, 분자구조, Conjugate Polymer doping
- 고분자의 전기전도, 전하이동(분자내vs분자간)
- 저분자vs고분자 유기반도체 장단점 비교
- Conjugate Polyemr Doping, bandgap, conductivity
- Bandgap – 광흡수
- 유기반도체 분자 구조 설계(conjugate length)
- 유기반도체 분자 구조 설계(side group, 용해도)
- 단계성장중합 vs 연쇄성장중합
- 유기반도체와 전도성 고분자의 공통된 분자 특징
- 전도성 고분자의 p-doping, n-doping
- 유기반도체vs실리콘반도체 비교
- Stoichiometric, Non-stoichiometric 조건에서 중합도, 반응률 계산
- 라디칼 중합의 진행단계
- 전도성 고분자의 중합법 (화학적, 금속촉매기반, 전기화학적)
- Amorphous vs Crystalline
- Amorphous 고분자의 유리-고무 전이
- 전도성 고분자의 tacticity (Isotactic, Syndiotactic, Atactic), HH HT TT
- 전도성 고분자의 기계적 물성 조절 (결정성+전도도 vs 유연성) Trade-off











